Нарушение природной структуры белка называют дезактивацией. Качественные особенности живой материи. Уровни организации живого. Пространственная организация белковых молекул
1. Как называется процесс нарушения природной структуры белка, при котором сохраняется его первичная структура? Действие каких факторов может приводить к нарушению структуры белковых молекул?
Процесс нарушения природной структуры белков под влиянием каких-либо факторов без разрушения первичной структуры называется денатурацией. Денатурация происходит вследствие разрыва водородных, ионных, дисульфидных и других связей. При этом может утрачиваться их четвертичная, третичная и даже вторичная структура.
2. Чем фибриллярные белки отличаются от глобулярных? Приведите примеры фибриллярных и глобулярных белков
Данные белки отличаются по форме молекул. Молекулы глобулярных белков имеют округлую форму, фибриллярные белки характеризуются вытянутой, нитевидной формой молекул. Так, глобулярными белками являются глобулины и альбумины крови, фибриноген, гемоглобин. Фибриллярные белки - кератин, коллаген, миозин, эластин и др.
3. Назовите основные биологические функции белков, приведите соответствующие примеры.
Структурная функция. Белки входят в состав всех клеток и тканей живых организмов. Из белков построены элементы цитоскелета, сократительные элементы мышечных волокон. Преимущественно из белков состоят хрящи и сухожилия. В их состав входит белок коллаген. Важнейшим структурным компонентом перьев, волос, ногтей, когтей, рогов, копыт у животных является белок кератин.
Ферментативная (каталитическая) функция. Ферменты - это биологические катализаторы, т. е. вещества, ускоряющие протекание химических реакций в живых организмах. Ферменты участвуют в процессах синтеза и расщепления различных веществ. Они обеспечивают фиксацию углерода в процессе фотосинтеза, расщепление питательных веществ в пищеварительном тракте и т. д.
Транспортная функция. Многие белки способны присоединять и переносить различные вещества. Гемоглобин связывает и переносит кислород и углекислый газ.
Сократительная (двигательная) функция. Сократительные белки обеспечивают способность клеток, тканей, органов и целых организмов изменять форму, двигаться. Так, актин и миозин обеспечивают работу мышц и не мышечные внутриклеточные сокращения.
Регуляторная функция. Некоторые пептиды и белки являются гормонами. Они влияют на различные физиологические процессы. Например, инсулин и глюкагон регулируют содержание глюкозы в крови, а соматотропин (гормон роста) - процессы роста и физического развития.
Сигнальная функция. Некоторые белки клеточных мембран способны изменять свою структуру в ответ на действие внешних факторов. С помощью этих белков происходит прием сигналов из внешней среды и передача информации в клетку.
Защитная функция. Белки предохраняют организм от вторжения чужеродных организмов и от повреждений.
Токсическая функция. Многие живые организмы выделяют белки-токсины, которые являются ядами для других организмов. Токсины синтезируются в организме ряда животных, грибов, растений, микроорганизмов.
Энергетическая функция. После расщепления до аминокислот белки могут служить источником энергии в клетке. При полном окислении 1 г белка выделяется 17,6 кДж энергии.
Запасающая функция. В семенах растений запасаются резервные белки, которые используются при прорастании зародышем, а затем и проростком как источник азота.
4. Что такое ферменты? Почему без их участия протекание большинства биохимических процессов в клетке было бы невозможным?
Ферменты - это биологические катализаторы, т. е. вещества, ускоряющие протекание химических реакций в живых организмах. В отличие от обычных химических катализаторов ферменты обладают специфичностью, т. е. каждый фермент ускоряет только одну определенную реакцию или действует только на определенный тип связи.
5. В чем заключается специфичность ферментов? Какова ее причина? Почему ферменты активно функционируют лишь в определенном диапазоне температуры, рН и других факторов?
Ферменты ускоряют химические реакции за счет тесного взаимодействия с молекулами субстратов - исходных реагирующих веществ. С субстратом взаимодействует не вся молекула фермента, а лишь небольшой ее участок - активный центр. Чаще всего он образован несколькими аминокислотными остатками. Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные субстраты из-за соответствия их пространственных структур. Ферменты являются белками, поэтому активно работают лишь в определенном диапазоне рН, температуры и других факторов.
6. Почему белки, как правило, используются в качестве источников энергии лишь в крайних случаях, когда в клетках исчерпаны запасы углеводов и жиров?
Белки используются в крайнем случае, т. к. они входят в состав всех клеток и тканей живых организмов. Из белков построены элементы цитоскелета, сократительные элементы мышечных волокон.
7. У многих бактерий в процессах синтеза веществ, необходимых для нормального роста и размножения, участвует парааминобензойная кислота (ПАБК). В то же время в медицине для лечения ряда бактериальных инфекций используются сульфаниламиды - вещества, по структуре сходные с ПАБК. Как вы думаете, на чем основано лечебное действие сульфаниламидов?
ПАБК необходима для образования в микробной клетке факторов роста - фолиевой кислоты и пуриновых оснований, участвующих в построении нуклеиновых кислот, без которых рост и размножение микробов невозможны. По строению ПАБК напоминает сульфаниламиды, поэтому при избытке последних ее активность подавляется. Микробы, лишенные ПАБК, прекращают деление и рост, а затем добиваются защитными силами макроорганизма.
«Белка и Стрелка» - Белка и Стрелка дожили до глубокой старости и умерли своей смертью. Через некоторое время у Стрелки появились щенки. Одними из наиболее приспособившихся собак-претендентов были Белка и Стрелка. 19 августа 1960 года был совершён успешный запуск космического корабля-спутника на орбиту. Все шесть щенков были здоровы.
«Белки урок» - Качественные реакции. Общие свойства белков. Четвертичная структура белковой молекулы. Биуретовая Ксантопротеиновая HNO3 NaOH CuSO4. Содержание белков в организме (в процентах к сухой массе). Структура белковой молекулы. Белки. Функции белков. Содержание белков в пище. Что такое жизнь?
«Биосинтез белка» - Незаменимые аминокислоты выделены жирным шрифтом. Участники биосинтеза молекул белка. Неправильный ответ. Содержание. Проверь себя. Схема растительной и животной клеток. Введение. Правильный ответ. Биосинтез белков в живой клетке. Процесс биосинтеза белков в живой клетке. Поставщики энергии для биосинтеза белков.
«Белки химия» - В состав слизи и синовиальной жидкости входят мукопротеиды. Определение. Строение полипептидной цепи. Содержание. Такую реакцию дают все соединения, содержащие пептидную связь. Последовательное соединение аминокислот при образовании белковой молекулы. Первичная структура белка при денатурации сохраняется.
«Белки и их функции» - Функции белков чрезвычайно многообразны. Строительный материал. Сократительные белки вызывают всякое движение. Химические свойства белков. Выработка белковых тел и антител для обезвреживания чужеродных веществ. Функции белка. Из белков построены кровеносные сосуды, сухожилия, волосы. Вторичная структура Третичная структура Четвертичная структура.
«Аминокислоты и белки» - Реакции?-аминокислот. Биуретовая реакция (с гидроксидом меди (II) Cu(OH)2) Нингидринная реакция. РАЗЛИЧНЫЕ ВАРИАНТЫ ИЗОБРАЖЕНИЯ СТРУКТУРЫ БЕЛКА КРАМБИНА. Отходы с оптически активным изомером a-аминокислоты. ОБРАЗОВАНИЕ ВНУТРИМОЛЕКУЛЯРНЫХ ВОДОРОДНЫХ СВЯЗЕЙ (изображены пунктирными линиями) в молекуле полипептида.
Классификация белков. По форме молекул белки можно разделить на две большие группы – глобулярные (имеют сферическую форму) и фибриллярные (удлиненной формы). Так, глобулярными белками являются глобулины и альбумины крови, фибриноген, гемоглобин. Фибриллярные белки – кератин, коллаген, миозин и др. (рис.)
Белки, образованные только аминокислотами, называются простыми . Сложными являются белки, имеющие в своем составе компонент неаминокислотной природы. Это могут быть ионы металлов (Fe, Zn, Mg, Mn), липиды, нуклеотиды, сахара и др. Простыми белками являются сывороточный альбумин крови, фибрин, некоторые ферменты (трипсин) и др. Сложными белками являются липопротеины и гликопротеины (например, иммуноглобулины), а также большинство ферментов.
Денатурация и ренатурация белков . Одно из основных свойств белков - способность изменять свою структуру и свойства под влиянием различных факторов (действие концентрированных кислот и щелочей, высокая температура и др.). Процесс нарушения природной конформации белков под влиянием каких-либо факторов без нарушения первичной структуры называется денатурацией (от лат. де - приставка, означающая потерю, и натура - природные свойства) (рис.). Изменение структуры белка происходит вследствие разрыва водородных и ионных связей, стабилизирующих пространственные структуры. При денатурации могут утрачиваться четвертичная, третичная и даже вторичная структура. Денатурация сопровождается потерей биологической активности белка. При этом наблюдается уменьшение растворимости белка, изменение формы и размеров молекул, потеря ферментативной активности и т.д. Денатурирующими агентами являются: высокая температура, кислоты и щелочи, мочевина, спирты, фенол, хлорамин, соли тяжелых металлов и др. Так, соли тяжелых металлов (кадмия, ртути и др.) при взаимодействии с белками образуют нерастворимые соединения, и белки выпадают в осадок.
Как правило, денатурация имеет необратимый характер. Хотя на первых ее стадиях, при условии прекращения действия повреждающих факторов, белок может восстановить свое первоначальное состояние. Это явление называется ренатурацией (от лат. ре - приставка, обозначающая возобновление). В организмах обычно наблюдается частичная обратимая денатурация белков.
Способность белков к обратимому изменению своей структуры в ответ на действие физических и химических факторов лежит в основе важнейшего свойства всех живых систем - раздражимости .
Под влиянием некоторых факторов (воздействие формалина, спирта, щелочей и др.) может происходит разрушение первичной структуры. Процесс разрушения первичной структуры белков, называемый деструкцией (от лат. де - и структура - строение), всегда необратимый.
Явление денатурации часто используется в биологических исследованиях и в медицине. При определении в биологическом материале низкомолекулярных соединений из раствора сначала удаляют белки. Для этого вызывают их денатурацию, осаждают или отфильтровывают.
В медицине денатурирующие агенты часто применяются для стерилизации медицинских инструментов и материалов в автоклавах (здесь денатурирующий агент – высокая температура). Их используют также в качестве антисептиков (спирт, фенол, хлорамин и др.) для очистки загрязненных материалов и поверхностей. То же происходит при обеззараживании ран, ссадин, царапин раствором йода или спиртом. На денатурации белков основано применение мышьяковистого ангидрида в стоматологической практике при лечении пульпита.
Функции белков. Большое разнообразие белков позволяет им выполнять в живом организме множество различных функций, как структурных, так и метаболических.
Структурная. Белки входят в состав всех биологических мембран и органоидов клетки. Преимущественно из белков состоят хрящи, сухожилия. В их состав входит белок коллаген . Кератин – компонент перьев, волос, ногтей, когтей, рогов, копыт у высших животных. Эластин является компонентом связок, стенок кровеносных сосудов.
Каталитическая (ферментативная). Белковые молекулы ферментов способны ускорять течение биохимических реакций в клетках живых организмов в сотни миллионов раз. Ферменты участвуют как в процессах синтеза, так и распада веществ. Они обеспечивают расщепление питательных веществ в пищеварительном тракте, фиксацию углерода при фотосинтезе и т.д.
Механизм действия ферментов объясняет теория активного центра . Согласно ей, в молекуле каждого фермента имеется один или более участков, в которых происходит тесный контакт между молекулами фермента и специфического вещества - субстрата (рис.). Активным центром выступает функциональная группа (например, ОН-группа серина), отдельная аминокислота либо сочетание нескольких (в среднем от 3 до 12), расположенных в определенном порядке аминокислотных остатков. Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные субстраты в силу точного соответствия их пространственных структур (как ключ и замок).
Молекула фермента вызывает ослабление определенных химических связей субстрата, и катализируемая реакция происходит с меньшими начальными затратами энергии, а следовательно, с намного большей скоростью. Ферменты ускоряют ход реакции без изменения ее общего результата за счет снижения энергии активации , т.е. в их присутствии затрачивается значительно меньше энергии для придания молекулам реакционной способности.
На заключительном этапе химической реакции фермент-субстратный комплекс распадается с образованием конечных продуктов и свободного фермента, который сохраняет исходную структуру и свойства. Освободившийся при этом активный центр может принимать следующие новые молекулы субстрата. Именно поэтому ферменты требуются в крайне низких концентрациях.
Некоторые ферменты, помимо активного центра, имеют один или несколько регуляторных центров. С этими участками могут связываться молекулы, регулирующие активность фермента. Они носят название активаторов (от лат. активус - деятельностный).
Молекулы некоторых веществ, взаимодействуя с ферментом, снижают или блокируют его активность (рис.). Такие вещества называются ингибиторами (от лат. ингибео – сдерживаю, останавливаю) . Например, многие лекарственные препараты природного или синтетического происхождения являются ингибиторами определенных ферментов. Кроме того, в основе действия некоторых токсических веществ лежит ингибирование активного центра ферментов.
Транспортная. Многие белки способны присоединять и переносить различные вещества. Гемоглобин связывает и переносит кислород и углекислый газ. Альбумины крови транспортируют жирные кислоты, глобулины - ионы металлов и гормоны. Молекулы белков, входящие в состав цитоплазматической мембраны, принимают участие в транспорте веществ в клетку и из нее.
Сократительная (или двигательная). Сократительные белки обеспечивают способность клеток, тканей, органов и целых организмов изменять форму, двигаться. Так, актин и миозин – обеспечивают работу мышц и немышечные внутриклеточные сокращения. Белок тубулин входит в состав микротрубочек веретена деления, ресничек и жгутиков эукариотических клеток.
Регуляторная . Некоторые пептиды и белки являются гормонами. Они влияют на различные физиологические процессы. Например, инсулин регулирует содержание глюкозы в крови. Глюкагон регулирует расщепление гликогена до глюкозы, повышая ее содержание в крови.
Сигнальная. Некоторые белки клеточных мембран способны изменять свою структуру в ответ на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача информации в клетку. Примером может служить фитохром - светочувствительный белок, регулирующий фотопериодическую реакцию растений, и onсин - составная часть пигмента родопсина, находящегося в клетках сетчатки глаза.
Защитная. Специфические белки предохраняют организм от вторжения чужеродных организмов и от повреждений. Так в ответ на проникновение чужеродных тел - антигенов - в клетке вырабатываются антитела - особые белки, называемые иммуноглобулинами, которые обеспечивают иммунитет. Интерфероны защищают организм от вирусной инфекции. Фибриноген , тромбопластин и тромбин участвуют в свертывании крови и предотвращении кровопотери.
Токсическая. Многие живые существа в качестве собственной защиты выделяют белки, называемые токсинами , которые в большинстве случаев являются ядами для других организмов. Токсины синтезируются в организме некоторых змей, лягушек, насекомых, грибов, растений, бактерий. В свою очередь, некоторые организмы способны вырабатывать антитоксины , которые подавляют действие этих ядов.
Энергетическая. Белки могут служить источником энергии в клетке (после гидролиза). При полном окислении 1 г белка выделяется 17,6 кДж энергии. Белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы углеводов и жиров.
С белками могут взаимодействовать некоторые вещества и подавлять их функции. Такие вещества называются ингибиторами. Ингибиторами белковых функций являются многие яды. Так, например, ингибиторами белков-рецепторов постсинаптической мембраны, которые связываются с медиатором ацетилхолином при передаче нервного импульса в синапсах, являются мускарин (токсин мукора) и никотин . При этом нарушается проведение нервного импульса. Подобное действие оказывает также атропин – вещество, содержащееся в растениях красавки и белены. Атропин является ингибитором М-холинорецепторов. Учитывая, что связывание ацетилхолина с М-холинорецепторами вызывает сокращение многих гладких мышц, атропин используется как лекарственное средство, снимающее их спазм (спазмолитик). Однако при передозировке атропином могут наблюдаться двигательное и психическое возбуждение, галлюцинации, признаки понижения тонуса гладких мышц радужной оболочки глаз, бронхов, органов брюшной полости. Такой же эффект наблюдается при употреблении отваров белены (отсюда поговорка «белены объелся».
s1. Что общего и чем отличаются процессы денатурации и деструкции? 2. Чем обусловлено разнообразие свойств белков? 3 . Каковы основные биологические функции белков? 4. В чем состоит защитная функция белков? 5. Чем определяется двигательная функция белков? 6. Что такое ферменты? Почему без участия ферментов протекание большинства биохимических процессов в клетке было бы невозможным?
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода, кислорода,водорода и азота, в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:

Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .

Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между-CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация -глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
Гидролиз белка
Любой белок состоит из аминокислот. Общая формула аминокислот есть 2HN-CHR-COOH. При образовании белка создаётся дипептидная связь:
2HN-CHR1-COOH + 2HN-CHR2-COOH -> 2HN-CHR1-CO-NH-CHR2-COOH + H2O.
Соответственно для гидролиза белка нужно разорвать дипептидную связь:
2HN-CHR1-CO-NH-CHR2-COOH + H2O -> 2HN-CHR1-COOH + 2HN-CHR2-COOH
Для определения белков среди других веществ используют качественные реакции:
а) Ксантопротеиновая реакция (б-к + HNO 3)
б) Биуретовая реакция (белок +Cu(OH) 2)
3. О п ы т. Как распознать с помощью характерной реакции соль серной кислоты среди трех выданных растворов солей?
ВЫПОЛНЕНИЕ:
Взять пробы из трех пробирок
Добавить в каждую пробу раствор хлорид бария, т.к. он является реактивом на сульфат ион
В пробирке с солью серной кислоты выпадает белый осадок сульфата бария
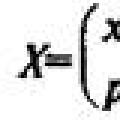 Сравнение законов распределения вероятностей
Сравнение законов распределения вероятностей Советский поэт Асадов Эдуард Аркадьевич: личная жизнь, творчество
Советский поэт Асадов Эдуард Аркадьевич: личная жизнь, творчество Лондон против всех Конфликт мирона и лсп
Лондон против всех Конфликт мирона и лсп