Атомный номер тулия. Географические названия химических элементов. Производство стекла. Тулий входит в состав различных оксидных материалов при производстве стекла и керамики для электроннолучевых трубок
Тулий ту́лий
(лат. Thulium), химический элемент III группы периодической системы, относится к лантаноидам. Назван от греческого Thúlē - Туле . Металл. Плотность 9,318 г/см 3 ; t пл 1545°C. Искусственно получаемый радиоактивный изотоп 170 Tm - источник мягкого рентгеновского излучения.
ТУЛИЙТУ́ЛИЙ (лат. Thulium, у античных географов Thule - крайний север мира), Tm (читается «тулий»), химический элемент с атомным номером 69, атомная масса 168,93421, ранее химический символ был Tu. В природе встречается один стабильный изотоп 169 Tm. Конфигурация трех внешних электронных слоев 4s 2 p 6 d 10 f 13 5s 2 p 6 d 0 6s 2 . Степени окисления +3, +2 (валентность III, II).
Расположен в группе IIIB в 6 периоде периодической системы элементов. Лантаноид (см.
ЛАНТАНОИДЫ)
.
Радиус атома 0,174 нм, радиус ионов (координационное число 6) Тu 3+ - 0,102 нм, Tu 2 + - 0,117 нм. Энергии последовательной ионизации 6,181, 12,05, 23,7, 42,7 эВ. Электроотрицательность по Полингу (см.
ПОЛИНГ Лайнус)
1,1.
История открытия
Открыт в 1879 шведским химиком П. Т. Клеве (см.
КЛЕВЕ Пьер Теодор)
, который выделил из минерала гадолинита оксид нового элемента. Идентифицировав элемент спектральным методом, Клеве назвал его в честь своей родины.
Нахождение в природе
Содержание в земной коре 2,7·10 -5 %. Входит в состав минералов: бастнезит (см.
БАСТНЕЗИТ)
, монацит (см.
МОНАЦИТ)
, лопарит (см.
ЛОПАРИТ)
,
ортит (см.
ОРТИТ)
,
ксенотим (см.
КСЕНОТИМ)
.
Получение
Тулий концентрируется с иттербием (см.
ИТТЕРБИЙ)
и лютецием (см.
ЛЮТЕЦИЙ)
.
Разделение и очистку проводят методами ионной хроматографии или экстракции.
Металлический тулий получают металлотермическим восстановлением TmF 3 с использованием кальция (см.
КАЛЬЦИЙ)
:
2TmF 3 +3Са=3СаF 2 +2Tm
или восстановлением Tm 2 O 3 металлическим лантаном (см.
ЛАНТАН)
:
Tm 2 O 3 +La=La 2 O 3 +Tm
Физические и химические свойства
Тулий - мягкий серебристо-серый металл. Существует в одной модификации с гексагональной кристаллической решеткой типа Mg, а
= 0,35375 нм, с =
0,55546 нм. Температура плавления 1545°C, кипения 1947°C, плотность 9,318 кг/дм 3 .
На воздухе компактный Tm устойчив. С галогенами (см.
ГАЛОГЕНЫ)
реагирует при нагревании, образуя TmF 3 и TmCl 3 . Тулий взаимодействует с минеральными кислотами с образованием солей тулия(III). Сильными восстановителями Tm 3+ восстанавливается до Tm 2+ .
Прокаливая на воздухе при 800-900°C нитрата Tm(NO 3) 3 , оксалата Tm 2 (C 2 O 4) 3 , сульфата Tm 2 (SO 4) 3 и других соединений Tm (III) образуется оксид тулия Tu 2 O 3 .
Применение
Тулий используют как активатор некоторых люминофоров и лазерных материалов, применяют при синтезе искусственных гранатов.
Энциклопедический словарь . 2009 .
Синонимы :Смотреть что такое "тулий" в других словарях:
- (Tulium), Tm, химический элемент III группы периодической системы, атомный номер 69, атомная масса 168,9342; относится к редкоземельным элементам; металл. Открыт шведским химиком П. Клеве в 1879 … Современная энциклопедия
- (лат. Thulium) Tm, химический элемент III группы периодической системы, атомный номер 69, атомная масса 168,9342, относится к лантаноидам. Название от греч. Thule Туле. Металл. Плотность 9,318 г/см³, tпл 1545 .С. Искусственно получаемый… … Большой Энциклопедический словарь
- (от греч. Thule Tуле, y античных географов крайний северный предел мира; лат. tulium * a. thulium; н. Thulium; ф. thulium; и. tulio), Tm, хим. элемент III группы периодич. системы Mенделеева, ат.н. 69, ат. м. 168,9342, относится к… … Геологическая энциклопедия
- (лат. Tulium), Tm, хим. элемент III группы пе риодич. системы элементов, ат. номер 69, ат. масса 168,9342; относится к лантаноидам. В природе представлен стабильным 169 Тm. Конфигурация внеш. электронных оболочек Энергии последоват. ионизации… … Физическая энциклопедия
Сущ., кол во синонимов: 3 лантаноид (15) металл (86) элемент (159) Словарь синонимов ASIS … Словарь синонимов
Тулий - (Tulium), Tm, химический элемент III группы периодической системы, атомный номер 69, атомная масса 168,9342; относится к редкоземельным элементам; металл. Открыт шведским химиком П. Клеве в 1879. … Иллюстрированный энциклопедический словарь
69 Эрбий ← Тулий → Иттербий … Википедия
- (лат. Thulium), хим. элемент III гр. периодич. системы, относится к лантано идам. Назв. от греч. Туле (Thule) античного назв. крайних сев. стран. Металл. Плотн. 9,318 г/см3; tnл 1545 °С. Искусственный радиоактивный нуклид 170Тm источник мягкого… … Естествознание. Энциклопедический словарь
- (лат. thule полулегендарная страна, в древности считавшаяся северной оконечностью земли) хим. элемент из семейства лантаноидов, символ Tm (лат. thulium), металл. Новый словарь иностранных слов. by EdwART, 2009. тулий я, мн. нет, м. (… Словарь иностранных слов русского языка
Тулий - Смотри Тулий (Tm) … Энциклопедический словарь по металлургии
Книги
- Тускуланские беседы (кожаный переплет, золотой обрез) , Цицерон Марк Тулий. Трактат 171;Тускуланские беседы 187;- одно из величайших произведений Цицерона: пять философских бесед, которые посвящены Марку Бруту, всесторонне раскрывают проблему достижения счастья…
Тулий — 69
Тулий (Tm)-редкоземельный элемент
, атомный номер 69, атомная масса 168,93, температура плавления 1545ОС, плотность 9,346 г/см3.
Своё название, тулий получил в честь легендарной страны «Туле», которую древние географы считали самой северной землёй, что в наше время, соответствует по географическому местоположению, Скандинавскому полуострову. Тулий был открыт в 1879 году методом спектроскопии. Тулий-один из самых, незначительно распространённых лантаноидов в природе, кроме того, его очень трудно было выделить из смеси с другими РЗМ. Понадобилось несколько лет, что бы получить двадцатипроцентный концентрат тулия, а затем, повысить содержание тулия в нём до 99%. Сейчас, применяемый хроматографический метод разделения РЗМ, значительно упростил и ускорил получение оксидов тулия и, в дальнейшем, получение чистого металла. В чистом виде, тулий был получен в 1911 году.
Тулий –один из самых тяжёлых лантаноидов, его плотность близка к плотности меди и никеля.

Тулий— серебристо-белый мягкий
Тулий— серебристо-белый мягкий , ковкий, вязкий металл, на воздухе не окисляется, при нагреве во влажном воздухе-окисляется слабо. Реагирует с минеральными кислотами, при этом получаются соли тулия. Взаимодействует с галогенами и азотом при нагревании. В природе, тулий присутствует в таких минералах как: ксенотим, эвксенит, монацит, лопарит. Содержание в земной коре –2,7х10-5% от всей массы. В природных и техногенных видах сырья, оксид тулия содержатся исключительно редко — в эвдиалите-0,3%, а в других минералах —ещё меньше. У тулия получено 32 искусственных радиоактивных изотопа с разными периодами полураспада. В естественной природе встречается только один-тулий-169.
ПОЛУЧЕНИЕ.
После обогащения природных минералов, полученные концентраты из смеси РЗМ перерабатываются, в результате чего, тулий концентрируется с тяжёлыми лантаноидами-иттербием и лютецием. Разделение и рафинирование производят экстракцией или ионообменной хроматографией с использованием комплексонов (органических веществ, образующих комплексные соединения с ионами металлов). Металлический тулий получают термическим восстановлением фторида тулия TmF3-кальцием, или оксида тулия Tm2O3-лантаном. Тулий получают, также, при нагревании нитратов, сульфатов и оксалатов тулия на воздухе до 800-900ОС.
ПРИМЕНЕНИЕ.
Несмотря на малую распространённость в природе и высокую стоимость, тулий, в наше время, начал сравнительно широко применяться в науке и промышленности.
Медицина. Изотоп тулия –тулий-170, обладающий мягким гамма-излучением, используется для создания приборов диагностики, особенно, для мест человеческого тела, труднодоступных для обычного рентгеновского аппарата. Эти радиопросвечивающие приборы с радиоактивным тулием просты и легко применимы в медицинской практике.
Лазерные материалы. Ионы тулия применяются для генерации инфракрасного лазерного излучения. Пары металлического тулия применяются для возбуждения лазерного излучения с изменяемой частотой(длиной волны). Тулий применяется для изготовления лазерных материалов, а также, для изготовления синтетических гранатов.
Магнитные носители. Металлический тулий применяется для производства феррогранатов для создания носителей информации.
Материалы термоЭДС. Монотеллурид тулия обладает высоким уровнем термоЭДС при высоком КПД термопреобразователей, однако, широкое применение тулия в качестве термоэлементов сдерживается высокой его стоимостью.
Полупроводники. Теллурид тулия применяется как модификатор для регулирования полупроводниковых свойств теллурида свинца.
Атомная энергетика. Борат тулия применяется как добавка к специальным эмалям для защиты от нейтронного излучения.
Сверхпроводники. Соединения тулия входят в состав материалов высокотемпературных сверхпроводников.
Производство стекла. Тулий входит в состав различных оксидных материалов при производстве стекла и керамики для электроннолучевых трубок.
-
Ту́лий (лат. Thulium) - химический элемент побочной подгруппы третьей группы шестого периода периодической системы химических элементов . Обозначается символом Tm, атомный номер - 69, относится к группе лантаноидов. Простое вещество тулий (CAS-номер 7440-30-4) представляет собой легко обрабатываемый металл серебристо-белого цвета.
История
Тулий был открыт шведским химиком П. Т. Клеве в 1879 году при поиске примесей к оксиду эрбия Er 2 O 3 . Этот же метод ранее позволил К. Г. Мосандеру открыть другие редкоземельные элементы. При выделении примесей Клеве получил два окисла - коричневый оксид гольмия и зелёный оксид тулия. В 1911 году Т. У. Ричардс получил элемент в чистом виде и измерил его атомный вес.
Выделив оксид неизвестного элемента, П. Т. Клеве дал ему название Thulium в честь расположенного на севере Европы легендарного острова Туле (др.-греч. Θούλη, лат. Thule), древнего названия Скандинавии.Получение
Металлический тулий получают металлотермическим восстановлением TmF 3 с использованием кальция: 2TmF 3 + 3Ca = 3CaF 2 + 2Tm
Распространённость в природе
Тулий является редким элементом, его содержание в земной коре 2,7 ×10 -5 масс. %, в морской воде - 10 -7 мг/литр. Наряду с другими редкоземельными элементами тулий присутствует в таких минералах как ксенотим, эвксенит, монацит, лопарит и некоторых других.
(Thulium; от лат. назв.Скандинавии - Thule), Tm - химический элемент III группы периодической системы элементов; ат. н. 69, ат. м. 168,9342; относится к редкоземельным элементам. Металл светло-серого цвета. В соединениях проявляет степень окисления +3 ( >3). Известны с массовыми числами от 165 до 175. Из них практическое значение имеет изотоп 170Тm. Открыл тулий (1879) швед, химик П. Клеве.
Металлический тулий впервые получили амер. ученые Ф. Спеддинг и А. Даан. Содержание тулия в земной коре 8·10 -5 %. Основным минералами для получения тулия служат и эвксенит. Кристаллическая решетка тулий гексагональная плотно-упакованная типа магния, с периодами а = 3,5374 А и с = 5,558 А. Плотность (т-ра 25° С) 9,314 г/см3; tпл1545°С; tкип 1727°С; коэффициент термического расширения 13,3-10-6 град; теплоемкость 6,46 кал/г-атом град; электрическое сопротивление 90 мком-см; точка 22 К; работа выхода электронов 3,12 эв. Модуль норм, упругости 7710 кгс/мм2; модуль сдвига 3100 кгс/мм2; коэфф. Пуассона 0,235; НВ = 55 (металла 99,0%).
Тулий легко поддается механической обработке. Химически активен. На воздухе сильно окисляется. Образует и соединения со мн. элементами. Тулий получают металлотермическим восстановлением окислов лантаном при т-ре 1000- 1500° С. Для получения чистого металла тулий дистиллируют. Тулий выпускают в виде небольших слитков. Изотоп 170Тm находит применение в портативных рентгенопросвечивающих аппаратах.
Лит.: Герасимовский В. И. Геохимия редкоземельных элементов. В кн.: Редкоземельные элементы (Получение, анализ, применение).
Статья на тему Тулий химический элемент
Легко поддается обработке и имеет серебристо-белый цвет. Несмотря на его редкость и высокую цену, тулий применяется в перспективных твердотельных лазерах и в виде радиоизотопа в портативных рентгеновских аппаратах.
1. История
Туллий был открыт шведским химиком Пером Теодором Клеве в как примесь к оксидов других редкоземельных элементов (был использован метод, которому было предложено Карлом Густавом Мозандером для поиска и выделения новых редкоземельных элементов). Клеве отделил все известные примеси из эрбия - "земли" (оксида) элемента ( 2 3). После дополнительных процедур Клеве выделил две новые субстанции: одну коричневого цвета, другую зеленого. Коричневой была земля, которую Клеве предложил назвать "гольмию" и которая соответствует элементу гольмий , зеленый же землю он назвал "Туллия" и новой элемент Туле в честь Thule, латинского названия Скандинавии .
Туллий был настолько редким, что у одного из ранних исследователей не было его в достаточном количестве, чтобы иметь возможность его достаточно очистить, чтобы увидеть зеленый цвет его соединений, им приходилось радоваться хотя бы потому, что характерные спектральные линии тулия усиливались, когда из образца постепенно удаляли эрбий . Первым исследователем, получил достаточно чистую тулия (оксид тулия), был Чарльз Джеймс, из колледжа в Дареме , Нью-Гемпшир . В 1911 он сообщил о том, что фракционная кристаллизация бромата позволила ему выделить чистый материал. Он провел 15 000 "операций" кристаллизации для установки гомогенности его материала.
Оксид тулия высокой чистоту впервые стал коммерчески доступен с конца 1950-х, в результате совершенствования метода ионно-обмена технологий разделения. Подразделение Lindsay Chemical Division фирмы American Potash & Chemical Corporation предложила сорта 99% и 99,9% чистоты. Цена за килограмм колебалась между US $ 4600 и $ 13300 в период с к для препарата 99,9% чистоты, это была самая высокая цена на лантаноидов после лютеция .
2. Распространенность и производство
Этот элемент никогда не встречается в природе в свободном состоянии, однако он содержится в небольших количествах в минералах с другими редкоземельными элементами. Его содержание в земной коре составляет 0,5 мг / кг. Туллий в основном добывают из монациту (~ 0,007% тулия) - руды, содержащийся в некоторых песках, с помощью технологий ионного обмена. Новые ионно-обменные технологии и технологии экстракции с помощью органических растворителей позволили эффективно и более легко выделять тулий, сокращая расходы на его добычу. Главным источником тулия на сегодня глинистые месторождения южного Китая. В таких минералах, где иттрий составляет 2/3 от всего редкоземельного компонента руды, всего 0,5% тулия. После выделения Металл может быть выделенным путем восстановления его оксида лантаном или кальцием в закрытом реакторе при высоких температурах. По другому методу, тулий восстанавливают с фторида металлотермическим кальцием:
2TmF 3 + 3Ca = 3CaF 2 + 2Tm3. Химические свойства
Тулий медленно, а при высокой температуре активно реагирует с кислородом воздуха с образованием тулий (III) оксида:
4 Tm + 3 O 2 → 2 Tm 2 O 3
Медленно реагирует с водой, однако реакция ускоряется при нагревании с образованием гидроксида:
2 Tm + 6 H 2 O → 2 Tm (OH) 3 + 3 H 2 2 Tm + 3 F 2 → 2 TmF 3 [соль белого цвета] 2 Tm + 3 Cl 2 → 2 TmCl 3 [соль желтого цвета] 2 Tm + 3 Br 2 → 2 TmBr 3 [соль белого цвета] 2 Tm + 3 I 2 → 2 TmI 3 [соль желтого цвета]
4.2. Источники рентгеновского излучения
Несмотря на свою высокую стоимость, в портативных рентгеновских аппаратах в качестве источника излучения используются тулий, который был облученного нейтронами в ядерном реакторе. Эти источники активны в течение примерно одного года, как инструмент в мобильных медицинских и стоматологических пунктах, а также для выявления дефектов в труднодоступных механических и электронных компонентах. Такие источники не требуют серьезного радиационной защиты - достаточно небольшого покрытие из свинца.
5. Биологическая роль и предостережения
Биологических роль тулия не известна, хотя было отмечено, что он несколько стимулирует обмен веществ. Растворимые соли тулия есть немного токсичными, если их введено в организм в больших количествах, но нерастворимые соли нетоксичны. Туллий не всасывается корнями растений, и поэтому не попадает в пищевую цепь человека. Овощи обычно содержат только один миллиграмм тулия за тонну сухого веса).
Литература
- Глоссарий терминов по химии / / Й.Опейда, О.Швайка. Ин-т физико-органической химии и углехимии им.. Л.М.Литвиненка НАН Украины, Донецкий национальный университет - Донецк: "Вебер", 2008. - 758 с. ISBN 978-966-335-206-0
Дефектоскопия. Радиоактивный изотоп, тулий-170, применяется для дефектоскопии лёгких цветных металлов и их сплавов, а также тонких стальных пластин толщиной до 2 мм. Алюминиевые изделия толщиной до 70 мм легко просвечиваются изотопом тулия-170, что позволяет найти в них мельчайшие дефекты. При этом применяется фотоэлектрическое устройство, использующее гамма-излучение тулия и дающее сверхконтрастное изображение объекта обследования. Готовят тулий-170, облучая нейтронами окись тулия, которая помещается в ампулу из алюминия и впоследствии используется вместе с ней.
 Могильники Чернобыля: радиоактивные отходы зоны отчуждения Где находится техника чернобыля
Могильники Чернобыля: радиоактивные отходы зоны отчуждения Где находится техника чернобыля Девочка заговорила на иностранном языке после комы
Девочка заговорила на иностранном языке после комы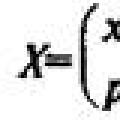 Сравнение законов распределения вероятностей
Сравнение законов распределения вероятностей